Un estudio del Instituto de Neurociencias identifica un mecanismo clave en la degeneración de las neuronas motoras en ELA
30 abril 2026
La esclerosis lateral amiotrófica (ELA) es una enfermedad neurodegenerativa que provoca la pérdida progresiva de las neuronas motoras, lo que conduce, en la mayoría de los casos, a un fallo respiratorio en un plazo de entre tres y cinco años desde el diagnóstico. En este contexto, un equipo del Instituto de Neurociencias, centro mixto de la Universidad Miguel Hernández (UMH) y del Consejo Superior de Investigaciones Científicas (CSIC), ha identificado que un sistema celular de ‘limpieza selectiva’ de proteínas, la autofagia mediada por chaperonas, está significativamente reducido en pacientes, lo que lo sitúa como una posible diana terapéutica para frenar la progresión de la enfermedad.
El estudio, publicado en la revista Acta Neuropathologica Communications, ha contado con la participación del Centro de Investigación del Deporte de la UMH y del Instituto Murciano de Investigación Biosanitaria Pascual Parrilla (IMIB). En este trabajo, el equipo ha profundizado en el papel de este mecanismo celular, responsable de eliminar proteínas dañadas de forma selectiva. Su correcto funcionamiento resulta esencial para mantener el equilibrio interno de las neuronas, por lo que su disfunción podría favorecer la acumulación de proteínas tóxicas, uno de los rasgos característicos de la enfermedad.
“La ELA es una enfermedad devastadora cuya causa sigue siendo desconocida en la gran mayoría de los pacientes, lo que dificulta enormemente el desarrollo de tratamientos eficaces”, explica el catedrático de la UMH Salvador Martínez, director del laboratorio Neurobiología de las enfermedades mentales, neurodegenerativas y neurooncológicas. Y explica que “identificar mecanismos celulares implicados directamente en la supervivencia de las neuronas es un paso fundamental para avanzar en nuevas estrategias terapéuticas”.
Las neuronas motoras son células especialmente vulnerables en la ELA. En más del 90% de los casos, estas células acumulan una proteína llamada TDP-43 fuera de su localización habitual, formando agregados tóxicos. El organismo dispone de mecanismos para evitar esta acumulación, entre ellos la autofagia, un sistema de ‘limpieza y reciclaje’ celular. Sin embargo, no todos los tipos de autofagia funcionan igual. Mientras que la macroautofagia actúa como un sistema general de eliminación de residuos, la autofagia mediada por chaperonas es altamente selectiva y se encarga de degradar proteínas concretas, como la TDP-43.
Para analizar este proceso, los investigadores utilizaron tejido de médula espinal procedente de pacientes incluidos en ensayos clínicos realizados por el equipo de científicos del Instituto de Neurociencias y el IMIB, así como muestras control de donantes sin enfermedad. Mediante técnicas de inmunohistoquímica e inmunofluorescencia, evaluaron la presencia de LAMP2A, una proteína clave que actúa como indicador de la actividad de este tipo de autofagia.
Los resultados muestran que las neuronas motoras sanas presentan una alta actividad de este sistema, mientras que en los pacientes con ELA esta actividad está notablemente reducida. “Estos datos indican que la actividad de la autofagia mediada por chaperonas está claramente disminuida en las neuronas motoras de los pacientes con ELA”, explica el investigador Daniel Garrigós García, primer autor del artículo. En esta línea, Martínez destaca: “En nuestro artículo hemos descrito que las motoneuronas necesitan niveles muy altos de autofagia mediada por chaperonas para sobrevivir. Cuando este mecanismo disminuye, como ocurre en la ELA, son precisamente estas células las que primero sufren y acaban muriendo”.
Este trabajo muestra, además, que las alteraciones observadas son específicas de limpieza y reciclaje de proteínas celulares y que presentan diferencias significativas entre pacientes y controles. “Hemos podido observar este mecanismo directamente en tejido humano, algo que no habíamos logrado en modelos animales”, señala Martínez, que destaca que el estudio ha sido posible gracias a la donación altruista de tejido por parte de pacientes y familias para el avance de la investigación en ELA.
 A partir de estos resultados, los investigadores plantean que este mecanismo podría convertirse en una nueva diana terapéutica. “Nuestro objetivo es intentar modular esta vía para aumentar su actividad”, explica el catedrático, y plantea que este hallazgo abre la puerta al desarrollo de estrategias dirigidas a ralentizar la progresión de la enfermedad, aunque aún se encuentran en fases iniciales de investigación.
A partir de estos resultados, los investigadores plantean que este mecanismo podría convertirse en una nueva diana terapéutica. “Nuestro objetivo es intentar modular esta vía para aumentar su actividad”, explica el catedrático, y plantea que este hallazgo abre la puerta al desarrollo de estrategias dirigidas a ralentizar la progresión de la enfermedad, aunque aún se encuentran en fases iniciales de investigación.
Este trabajo ha sido posible gracias a la financiación de la Agencia Estatal de Investigación, a través del programa ‘Severo Ochoa’ para Centros de Excelencia en I+D, el Ministerio de Ciencia, Innovación y Universidades, el programa Prometeo de la Generalitat Valenciana, el Instituto de Salud Carlos III (Red de Terapias Avanzadas-TERAV) y el programa Next Generation EU en el marco del Plan de Recuperación, Transformación y Resiliencia y, especialmente, a la Catedra sobre ELA Gregoria Ramos Gil de la UMH.
Artículo: Garrigos, D., Martinez-Morga, M., Pombero, A., García-Lopez, R., Pastor, D., Riquelme, D., Blanquer, M., Iniesta, F., Valdor, R., Geijo-Barrientos, E., Hargus, G., Moraleda, J.M & Martínez, S. 2026. Chaperone mediated autophagy is deficient in spinal motoneurons of ALS patients with TDP-43 proteinopathy. Acta Neuropathologica Communications, 14, 67. DOI: https://doi.org/10.1186/s40478-026-02238-6
Más información: https://youtu.be/sSX7WGTHlew?si=GEIXBYK-S2q3OHsC
Pie de foto 1: Los investigadores del Instituto de Neurociencias Francisca Almagro, Raquel García López, Ana Pombero, Daniel Garrigós, Marta Martínez y Emilio Geijo. Fuente: IN UMH-CSIC.
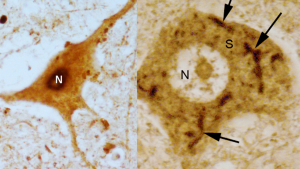
Pie de foto 2: Neuronas motoras de la médula espinal. A la izquierda, neurona motora sana, en la que la proteína TDP-43 (en negro) se localiza en el núcleo celular (N). A la derecha, neurona motora de un paciente con ELA, en la que la TDP-43 aparece acumulada de forma anómala en el citoplasma del cuerpo celular (S). Fuente: Acta Neuropathologica Communications
